Kaiyun官网医疗器械变更流程图轻松搞定II、III类审批!根据《医疗器械监督管理条例》的规定,中华人民共和国境内的医疗器械按照风险程度分为三类:第I类、第II类和第III类。
对于第II类医疗器械,它们具有中度风险,需要严格控制管理以保证其安全Kaiyun官网、有效的医疗器械。境内生产企业需要在所在地省(直辖市)药监局进行注册Kaiyun官网,而境外医疗器械生产企业需要委托境内代理人在国家药监局进行注册。
第III类医疗器械具有较高风险,需要采取特别措施严格控制管理以保证其安全、有效的医疗器械。无论境内、境外医疗器械生产企业均需要在国家药监局进行注册。
已注册的第二类、第三类医疗器械产品,如果其设计、原材料Kaiyun官网、生产工艺、使用范围、使用方法等发生实质性变化,有可能影响该医疗器械安全、有效的,注册人应向原注册部门申请办理变更注册手续。相反,如果发生非实质性变化,不影响该医疗器械安全、有效的,应当将变化情况向原注册部门备案。
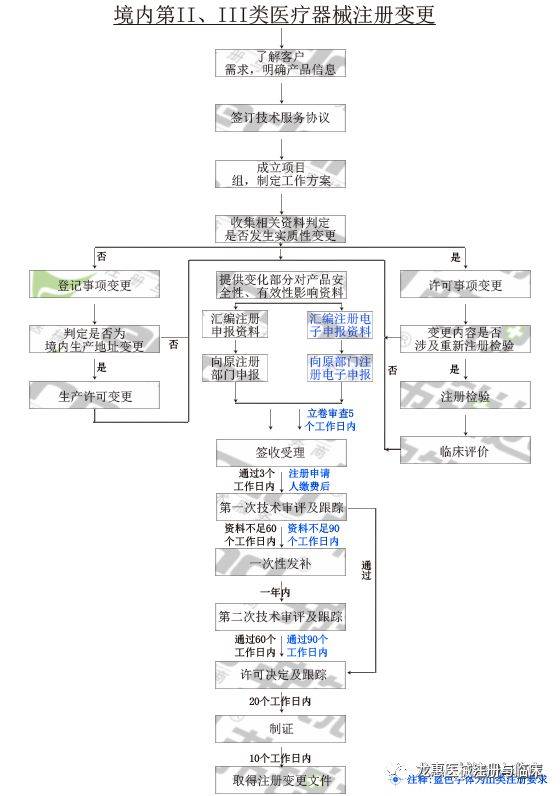
9、《境内第三类医疗器械注册质量管理体系核查工作程序(暂行)》(食药监械管〔2015〕63号)
Copyright © 2002-2023 开云(中国)Kaiyun官方网站 版权所有 Powered by EyouCms 备案号:京ICP备17070293号-1